Cho 8,96 lít khí H2 phản ứng với 7,84 lít khí Cl2 thu được V lít khí A. (thể tích các khí đo ở đktc)
a. Giá trị V = ?
b. Hòa tan lượng khí A trên vào 224,45gam nước thu được dung dịch B. Tính nồng độ % của dung dịch B
Hòa tan hết a gam bột Fe trong 100 ml dung dịch HCl 1,2M, thu được dung dịch X và 0,896 lít khí H2. Cho X tác dụng với lượng dư dung dịch AgNO3, sau khi kết thúc các phản ứng thu được V lít khí NO (sản phẩm khử duy nhất) và b gam chất rắn, (biết các khí đo ở đktc). Giá trị của b và V lần lượt là:
A. 18,3 và 0,448
B. 18,3 và 0,224
C. 10,8 và 0,224
D. 17,22 và 0,224
Hỗn hợp X gồm K, Al và Fe. Cho m gam X vào một lượng H2O dư, thu được 4,48 lít (đktc) khí H2 và chất rắn Y. Hòa tan hoàn toàn Y vào dung dịch HCl dư, thu được 8,96 lít (đktc) khí H2. Mặt khác, lấy m gam X cho vào dung dịch KOH dư, thu được 7,84 lít (đktc) khí H2. Các phản ứng xảy ra hoàn toàn. Xác định m.
Có V1 < V2 => khi X tác dụng với H2O thì Al còn dư.
Giả sử số mol 3 kim loại là: x, y, z.
K + H2O → KOH + ½ H2↑
x → x 0,5x
Al + KOH + H2O → KAlO2 + 1,5H2↑
x ← x→ 1,5x
→ 0,5x + 1,5x = 0,2 → x = 0,1
X tác dụng với KOH: 0,1 . 0,5 + 1,5y = 0,35 => y = 0,2
Khi cho X tác dụng với H2O còn dư Al => Y chứa Al dư và Fe
nAl dư = nAl ban đầu – nAl phản ứng = 0,2 – 0,1 = 0,1mol
=> 0,1 . 1,5 + z = 0,4 => z = 0,25mol
=> m = 23,3g
Cho 1,12 gam sắt vào 50 ml dd H2SO4 1M.Sau phản ứng thu được dung dịch A và khí H2 (đktc). a) Tính V lít khí H2?
b) Tính thể tích dung dịch H2SO4 phản ứng.
c) Tính nồng độ mol của các chất trong dung dịch A.( Thể tích dung dịch không thay đổi đáng kể)
\(n_{Fe}=\dfrac{1,12}{56}=0,02\left(mol\right)\)
\(n_{H2SO4}=0,05.1=0,05\left(mol\right)\)
Pt : \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
a) Xét tỉ lệ : \(0,02< 0,05\Rightarrow H2SO4dư\)
Theo Pt : \(n_{FeSO4}=n_{H2}=n_{Fe}=0,02\left(mol\right)\)
\(\Rightarrow V_{H2\left(dktc\right)}=0,02.22,4=0,448\left(l\right)\)
b) \(n_{H2SO4\left(dư\right)}=0,05-0,02=0,03\left(mol\right)\)
\(V_{ddH2SO4\left(dư\right)}=\dfrac{0,03}{1}=0,03\left(l\right)=30\left(ml\right)\)
c) \(C_{MFeSO4}=\dfrac{0,02}{0,05}=0,4\left(M\right)\)
\(C_{MH2SO4\left(dư\right)}=\dfrac{\left(0,05-0,02\right)}{0,05}=0,6\left(M\right)\)
Chúc bạn học tốt
1. Cho 5.1 gam hỗn hợp X gồm Al và Mg tác dụng vừa đủ với dung dịch HCl thấy khối lượng tăng lên 4.6 gam. Xác định số mol HCl tham gia phản ứng.
2. Hòa tan a gam hỗn hợp bột Mg, Al bằng dung dịch HCl thu được 17.92 lít khí H2 (đktc). Cùng lượng hỗn hợp trên hòa tan trong dung dịch NaOH dư thu được 13.44 lít khí H2 (đktc). Giá trị của a = ?.
3. Cho hỗn hợp X gồm 2 kim loại Al và Ba. Tiến hành 2 thí nghiệm :
*Thí nghiệm 1 : Cho m gam X vào nước dư thu được 1.344 lít H2 (đktc).
*Thí nghiệm 2 : Cho 2m gam X vào dung dịch Ba(OH)2 dư thu được 20.832 lít khí H2 (đktc).
Tìm giá trị của m.
4. X là hỗn hợp Ba và Al. Hòa tan m gam X vào lượng dư nước thu được 8.96 lít H2 (đktc). Cũng hòa tan m gam X vào dung dịch NaOH dư thì thu được 12.32 lít khí H2 (đktc). Xác định giá trị của m.
1. Cho 5.1 gam hỗn hợp X gồm Al và Mg tác dụng vừa đủ với dung dịch HCl thấy khối lượng tăng lên 4.6 gam. Xác định số mol HCl tham gia phản ứng.
2. Hòa tan a gam hỗn hợp bột Mg, Al bằng dung dịch HCl thu được 17.92 lít khí H2 (đktc). Cùng lượng hỗn hợp trên hòa tan trong dung dịch NaOH dư thu được 13.44 lít khí H2 (đktc). Giá trị của a = ?.
3. Cho hỗn hợp X gồm 2 kim loại Al và Ba. Tiến hành 2 thí nghiệm :
*Thí nghiệm 1 : Cho m gam X vào nước dư thu được 1.344 lít H2 (đktc).
*Thí nghiệm 2 : Cho 2m gam X vào dung dịch Ba(OH)2 dư thu được 20.832 lít khí H2 (đktc).
Tìm giá trị của m.
4. X là hỗn hợp Ba và Al. Hòa tan m gam X vào lượng dư nước thu được 8.96 lít H2 (đktc). Cũng hòa tan m gam X vào dung dịch NaOH dư thì thu được 12.32 lít khí H2 (đktc). Xác định giá trị của m.
Cho a gam hỗn hợp X gồm Mg và Al vào dung dịch HCl dư thu được 8,96 lít khí. Mặt khác, ở cho m gam hỗn hợp X tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể tích các khí đo ở đktc. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 7,8.
B. 6,45.
C. 10,2.
D. 14,55.
Cho a gam hỗn hợp X gồm Mg và Al vào dung dịch HCl dư thu được 8,96 lít khí. Mặt khác, ở cho m gam hỗn hợp X tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể tích các khí đo ở đktc. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 7,8
B. 6,45
C. 10,2.
D. 14,55.
Đáp án A
Gọi số mol Mg và Al lần lượt là x và y mol.
X phản ứng với HCl :
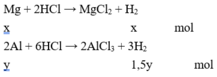
→ x + 1,5y = 0,4.
X tác dụng với NaOH chỉ có Al phản ứng :
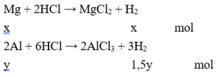
Giải hệ phương trình được x = 0,1 và y = 0,2.
a = 0,1.24 + 0,2.27 = 7,8 gam.
Cho m gam hỗn hợp A gồm Al và Fe3O4. Nung A trong khí trơ, nhiệt độ cao để phản ứng xảy ra hoàn toàn thu được hỗn hợp B. Nghiền nhỏ hỗn hợp B, trộn đều, chia làm hai phần không bằng nhau:
+ Phần 1 (phần ít): Tác dụng với dung dịch NaOH dư thu được 1,176 lít khí H2. Tách riêng chất không tan đem hòa tan trong dung dịch HCl dư thu được 1,008 lít khí.
+ Phần 2 (phần nhiều): Cho tác dụng với dung dịch HCl dư thu được 6,552 lít khí.
Giá trị của m và thành phần phần trăm khối lượng của một chất có trong hỗn hợp A (thể tích các khí đo ở đktc) gần giá trị nào nhất sau đây?
A. 22 và 63%.
B. 23 và 64%.
C. 23 và 37%.
D. 22 và 36%.
Giải thích:
Ở phần 1 khi cho tác dụng với NaOH có sinh ra khí H2 => nhôm dư
Phần 1
nH2 = 0,0525 mol => nAl dư = 0,035 mol
chất rắn không tan tác dụng với HCl => nH2 = 0,045 mol => nFe = 0,045 mol
Phần 2
nH2 = 0,2925 mol
Giả sử phần 2 = k. phần 1
Bảo toàn e ở phần 2 ta có (3 . 0,035 + 2 . 0,045) . k = 2 . 0,2925 => k = 3
Có mA = mB = 4 khối lượng phần 1
=> tổng lượng H2 ở thí nghiệm 1 = 4 . (0,0525 + 0,045 ) = 0,39
=> nFe3O4 = (4 . 0,045) : 3 = 0,06 mol
=> 3nAl = 2.nFe3O4 + 2nH2 => nAl = 0,3 mol
=> mA = 0,3 . 27 + 0,06 . 232 = 22,02 mol
%Al = 37% và %Fe3O4 = 63%
Đáp án A
Cho 6.5 gam Zn tác dụng vừa đủ với 100ml dung dịch HCl thu được V lít khí H2 ở dkc a) Tính giá trị V và khối lượng muối thu được sau phản ứng b) Tính nồng độ mol của dung dịch acid đã dùng c) Dẫn toàn bộ lượng khí H2 thu được ở trên đi qua 12g bột CuO đun nóng. Tính khối lượng chất rắn thu được sau phản ứng
a, \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
____0,1_____0,2______0,1_____0,1 (mol)
\(V_{H_2}=0,1.24,79=2,479\left(l\right)\)
\(m_{ZnCl_2}=0,1.136=13,6\left(g\right)\)
b, \(C_{M_{HCl}}=\dfrac{0,2}{0,1}=1\left(M\right)\)
c, \(n_{CuO}=\dfrac{12}{80}=0,15\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Xét tỉ lệ: \(\dfrac{0,15}{1}>\dfrac{0,1}{1}\), ta được CuO dư.
Theo PT: \(n_{CuO\left(pư\right)}=n_{Cu}=n_{H_2}=0,1\left(mol\right)\Rightarrow n_{CuO\left(dư\right)}=0,05\left(mol\right)\)
⇒ m chất rắn = mCuO (dư) + mCu = 0,05.80 + 0,1.64 = 10,4 (g)